药品专利期补偿制度全景解读:国内试点五大建议
发表时间:2018-01-25 来自:互联网
为保护药物创新,鼓励创新药早日进入我国市场,满足公众日益增长的用药需求,《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》提出:开展药品专利期限补偿制度试点。选择部分新药开展试点,对因临床试验和审评审批占用有效专利期的时间,给予适当专利期限补偿。这是我国药品领域的重要制度创新。有必要借鉴国际经验,加快建立药品专利期补偿制度。
阿伯拉罕•林肯认为:“专利制度是给天才之火浇上利益之油。”药品专利期为什么要予以补偿?
由于药品是一种特殊商品,药品的核心专利多在药品研发的早期或中期阶段提出申请并获得授权,专利期一般为20年,而创新药研发一般需要10年左右时间,在药物研究和审评审批过程中,有效专利期有一定的占用,有研究表明:药品上市时专利期平均剩余仅为6-9年。为了鼓励制药行业创新药研发积极性,通过给予适当的专利期补偿使企业药品研发投入回报预期最大化,从而促进创新药研发的持续投入,抵抗威胁人类健康疾病的威胁。
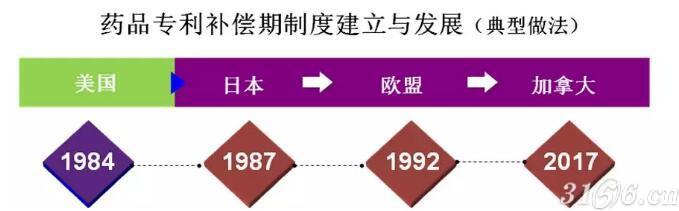
美国于1984年Hatch-Waxman法案率先建立专利期补偿制度。随后,日本、欧盟、澳大利亚、以色列、韩国、俄罗斯和中国台湾等均建立专利期补偿制度,制度的设计各有差别,鼓励创新药研发的侧重点和效果也各有不同。
建立有深意
1、产业角度:激励药物创新
创新药研发具有高投入、高风险,长周期的特点。制药产业的研发投入强度很大程度上受研发投入回报预期影响,而研发投入回报预期又是由创新药上市后的市场垄断时间和市场需求决定的。延长专利期就是延长创新药的市场垄断时间,从而提高企业获利预期,促进企业持续不断的研发投入,持续鼓励药物创新。
在20世纪初期,欧州制药工业协会的一项研究结论是,Hatch-Waxman法案已经使欧洲完全失去了在药品创新领域的传统领导地位,实现创新药研发基地从欧洲向美国的战略转移,美国制药产业处于国际领先水平。日本在1987年引入专利期补偿制度后,强化药品专利保护,制药产业逐步实现由“仿”到“创”的战略转移。
2、贸易角度:鼓励创新药入华
当前,创新药已经界定为“全球新”,即“我国境内外均未上市的创新药”。创新药通常受到基本专利和外围专利的重重保护。我国进行的审评审批改革已经基本解决药品审评积压,审评审批效率大大提高,加之我国的人口众多,尚未满足治疗需求的创新药研发潜力巨大,如果对新药给予适当的药品专利期补偿,可以大大提高我国作为创新药上市首选地点的吸引力,促进创新药尽早进入我国市场,满足我国广大人民群众尚未满足的治疗需求,造福百姓。
3、审评审批角度:推进审评审批提效
药品专利期补偿期受到多重限制,一般情况下,补偿期不超过5年,且批准上市后药品有效专利期有上限限制,通常为14年,也就是说药品专利期延长的时限是临床试验和审评审批合理占用的时间,而不包括不合理的延误,如因为未尽责而延误的时限。这种限制促使申请人在提交申请和补充资料的过程中更加认真,严谨,尽量符合审评要求,从而提高申报资料的质量,减少因申请人未尽责造成的审评延误,审评机构也会严格审评时限,提高审评审批效率。
国外做法
1、美国
1984年,美国通过Hatch-Waxman 法案,其建立了创仿平衡机制,其中鼓励创新的主要制度设计就是药品专利期延长制度(PTE),即用延长一段专利期的方式补偿在临床试验和药品上市审评(NDA)阶段占用的时间。
2、日本
为了鼓励创新药研发,1987 年日本对《专利法》进行修订,建立药品专利期限延长制度,用于补偿因获得上市审评而无法实施专利的时间。日本东京大学的一项研究显示,在日本近年来的21个重磅炸弹药品中,15个均为日本本土企业生产的药品,这15个重磅炸弹药品在专利期延长中获益,从初始获批上市到仿制药上市的独占期分别为11年到21年不等。
3、欧盟
欧盟1992年发布EC法规1768/1992《补充保护证书法案》,为药品提供补充保护证书(SPCs),即对符合要求的药品专利给予一定的专利延长期。2009年5月6日颁布了法规(EC)469/2009,对SPC法案进行修订。
4、加拿大
2017年2月,加拿大与欧盟签订《全面经济与贸易协议》(CETA),为满足该协议要求,加拿大于9月1日发布《专利法补充保护证书法规》。与其他国家不同,加拿大的CSP制度是由加拿大卫生部受理、批准和颁发证书的。
纠正错误认识
误区一:
只利于外国企业
药品专利期补偿本身没有针对国外企业的倾向性,药品专利是否符合补偿条件,取决于药品在境内批准上市的情况,有效专利情况,专利期补偿规则。从不同国家看,专利延长规则各有不同,以美欧为代表通过专利补偿制度鼓励突破性创新药研发,而日本在专利延长规则上作出适度调整,本土企业创新能力和盈利能力得到大幅提升。
误区二:
源于审评审批效率低下
药品专利期补偿并非补偿由于审评审批效率低下而延误的专利期,而是对药品因需要获得审评上市而有效专利期减损的正常补偿。因为药品是特殊商品,药品上市必须经过严格的试验和审批,该过程是必然的、不可缺少的过程,占用一部分有效专利期,从国际经验看,这一过程正常占用的时间大约是5年左右,一般情况下,补偿期最长不超过5年,也是基于这样的考虑。
误区三:
阻碍仿制药上市
药品专利期延长后必然导致仿制药上市的延迟。需要注意的是药品专利期补偿制度不是一个单一制度,这一制度与专利链接和首仿独占制度、强制许可制度、数据保护制度共同作用,才能实现创仿平衡的目的。专利期延长制度可以鼓励突破性或改良型创新药研发,减少低水平重复的仿制,在专利期和专利延长期内,仿制药申请人还可以通过专利挑战、强制许可或签署专利和解协议等方式,加快仿制药上市,实现创仿的动态平衡。
药品专利补偿制度的要素
制度设计的基本要素
1、专利补偿的产品范围和专利范围
纳入补偿范围的产品和专利类型具有鼓励创新的导向作用,各国的专利期补偿范围不同,创新导向性也不同。从鼓励药品创新的角度,美国和欧盟、加拿大等更鼓励突破性创新,而日本则既鼓励突破性创新,也鼓励改良型创新。
专利补偿的产品范围原则上适用于所有因为必须经过研究或审评而占用有效专利期的产品,包括化学药品、生物制品、中药等等。补偿的专利范围主要是基本专利,包括产品专利和用途专利。
各国的制度设计不尽相同,主要差异设计在于制剂专利和工艺专利是否纳入补偿范围,美国、欧盟、加拿大等规定制剂专利和工艺专利不在补偿范围,但工艺定产品专利例外,也可以予以补偿。日本则把活性成分的工艺专利和制剂专利也纳入可以申请补偿的专利范围。欧盟还规定对于儿科适应症药品可以在延长专利期的同时获得额外增加6个月的补偿。
2、授予专利延长期的条件
授予专利延长期的条件一般应包括三个基本条件:产品在上市或销售使用前已通过监管机构的审评;该产品首次被批准上市或销售使用;申请提交前专利未到期。
授予专利的其他条件,不同的国家有不同的要求,美国要求,申请补偿专利期的专利必须是橘皮书中已经登记的专利。美国、欧盟和加拿大规定每个获得上市许可的药品的专利期只能延长一次。日本对于同一活性成分药品基于不同的上市许可的不同专利分别批准专利期补偿,即可以多次补偿专利期。
3、补偿期计算与设定
专利期补偿的核心是由于药品临床研究和审评审批占用的有效专利期。从国际经验看,有精确计算和推算两种思路,美国属于精确计算模式,而欧盟、日本和加拿大则采用推算计算模式,相对来说,后者操作更为简单,便于实施。
补偿方式的灵活性体现在补偿期的长短界定。补偿期的界定受三个要素限制,第一,单项专利补偿期不超过5年;第二,药品上市后有效专利期的最长时限,美国为14年,欧盟为15年,日本没有规定最长时限。第三,延长时限计算方式,各国标准不同。
美国的专利延长期=1/2临床试验时间+FDA上市申请审评时间-申请人未尽责时间。
日本药品专利期=药品上市批准日-[相关专利注册之日或临床研究开始之日(较晚的日期为准)]。由于日本允许药品的多个专利多次延长,药品上市后有效专利期没有上限,以武田制药的重磅炸弹药品亮丙瑞林为例,该药1992年获批上市,2013年仿制药才获批上市,专利维护的市场独占时间长达21年。
欧盟SPC专利延长期=首个获得欧盟成员国上市许可日-提交基本专利申请日-5年,即“有效专利期的减损期”,减损期超过5年或以上的药品,可获得SPC。同时如果符合儿科临床研究条件的,则可增加延长6个月专利期。
加拿大专利补偿期=药品获批上市日-专利申请日-5年-申请人延误期。专利补偿期最长不超过2年。
4、申请、批准程序
药品专利期补偿是以申请人的主动申请行为作为补偿的参考依据的,申请材料中应说明申请延长的药品专利,已获得上市许可情况,原专利编号、到期日,申请延长理由和关键时间节点等信息。
通常情况下,专利期补偿是专利授权的延伸,其主管机关为专利行政机关,在美国为专利与商标局(PTO),在日本为经济产业省特许厅(JPO,相当于专利局),在欧盟为各国专利管理部门。加拿大的《补充保护证书法规》规定,专利期补偿由加拿大卫生部负责管理,审查补偿期间可与专利管理部门进行沟通。在某种意义上,加拿大的专利期补偿更像是通过行政独占期形式实现专利期补偿目标,是一种不同于其他国家的专利补偿期设计。
关于申请专利期补偿的时限,各国普遍规定申请补偿必须在药品获得上市许可后的一段时间内提出申请,过期未提交丧失延长专利期资格。该申请时限美国规定60天,欧盟规定6个月,日本规定3个月。
关于补偿期审查的部门职责与分工,专利行政部门主管专利审查工作,药品监管部门是药品审评审批部门,两者职责划分与分工合作是补偿期审查的重点。通常情况下,精确计算情况下,涉及到药品监管部门进行临床试验批准日或开始日,审评期、申请人延误期确认,美国属于精确计算模式。而推算计算模式下,专利申请日或专利公开日、批准上市日是无争议事件节点,通常情况下,专利审查部门即可直接审查确定专利期限。欧盟、日本等,专利期补偿审查相对简化,不涉及或很少涉及药品监管机构的补偿期确认,审查时间相对较短。
5、补偿异议程序
为体现专利期补偿的公平公正性,在申请、审查、批准和公布专利补偿期间,可能存在不同利益相关方的异议,应建立异议程序,包括异议书面申请、异议沟通、非正式会议、正式会议、公开听证会等方式解决相关争议。
从美国和日本的补偿申请和决定过程看,均有申请公开和决定公开程序。
从欧盟和加拿大的补偿期计算方式看,异议较少,但也建立异议程序解决争议。
展开试点的思考与建议
一是有关补偿产品范围及专利范围。
我国纳入专利补偿试点的产品应以化学药品为主,以化学药品作为突破口,试点结束后扩展到全部产品范围。纳入补偿的专利范围为产品专利和用途专利,其中产品专利是指活性成分专利,包括单一成分或复方成分,活性成分的酯或盐。可延长的用途专利仅限于与已批准上市药品的用途一致的用途。试点期间暂时不考虑工艺专利的补偿问题。制剂专利可考虑给予补偿,但仅限于新型给药系统专利。
二是申请专利补偿的条件。
我国应规定符合以下条件的药品专利可以申请补偿:(1)产品在上市或销售使用前已通过监管机构的审评;(2)该产品首次被批准上市或销售使用;(3)申请提交前专利未到期。(4)必须是已上市药品目录集中已经登记的专利;(5)每个获批上市药品仅能选择一项专利申请补偿,且每个产品的专利补偿仅有一次机会。
三是专利补偿期的计算。
建议我国的专利补偿期=药品获批上市日-专利申请日-5年,规定单项专利补偿期上限不得超过5年,剩余有效专利期不得超过14年。由于获批上市日和专利申请日是确定的时限,不容易产生争议。专利补偿期也适用研究豁免侵权(Bolar例外)。
四是专利补偿期申请与批准。
在专利补偿期试点期间,应规定申请人向国家知识产权局提交专利补偿申请,以推算性计算方式确定专利补偿期限,减少药品监管部门的补偿期确认时间,提高专利补偿审查效率。国家知识产权局在受理和批准时应予以公示,并颁发专利期补偿证书。
五是建立专利补偿异议程序。
虽然上述建议的专利期补偿计算方式争议较少,但可能存在专利期是否应该补偿,申请专利补偿的专利是否符合补偿条件的争议,因此,建立专利期补偿异议程序是非常必要的,建议通过正式书面异议申请、公开、非正式会议沟通、公开听证等方式解决异议。
结语<<<
药品专利期补偿制度是一个鼓励创新的制度,从单个药品来看,会延迟原研药的仿制药进入市场,但其鼓励创新,吸引创新药尽快在我国上市的作用十分明显。该制度不是一个鼓励的制度,应予专利链接、数据保护、强制许可等制度共同设计,实现鼓励创新与促进仿制的双向平衡。
(来源:医药经济报)
资讯推荐
更多>>-
医保提高统筹层次会助力大医院进一步扩张
医药市场分析 2020-04-14
-
慢阻肺治疗用药:国产替代仍待时日
医药市场分析 2020-01-03
-
自主报价能否破解“救命药”短缺困局?
医药市场分析 2020-01-03

-
第二批集采“突袭”!33个品种引爆350亿市场!齐鲁、石药、恒瑞……谁会是大赢家
医药市场分析 2020-01-02

-
5大药品“霸屏”,这个注射剂亮了!医改大省药品销售大变天,信立泰、豪森“上位”
医药市场分析 2019-12-26
-
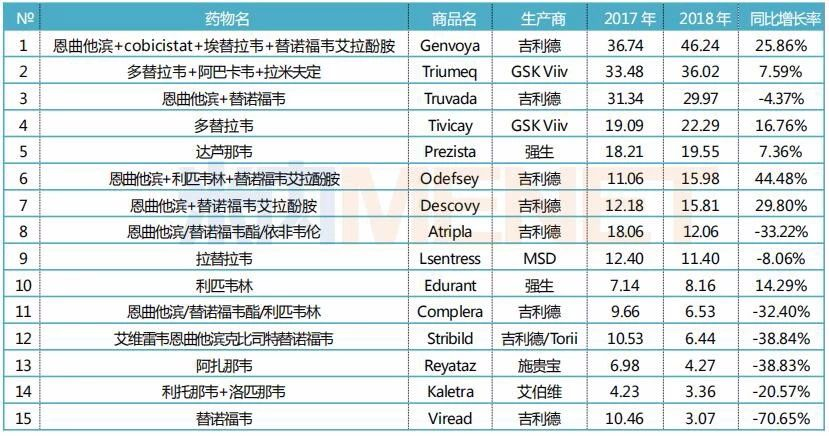
190亿抗病毒市场风云蝶变,10个抗艾新药入局排名大变更
医药市场分析 2019-12-26
-
2020年药店将出现这15个变化 药店集采扩面
医药市场分析 2019-12-26
-
医药流通企业需在5方面转型发力
医药市场分析 2019-12-26
-
新一轮医保谈判成果显著 但落地能否不打折扣?
医药市场分析 2019-12-19

-
400亿消化性溃疡药市场仅3个过评!奥赛康、正大天晴……“哄抢”5个超10亿注射剂
医药市场分析 2019-12-18
药品代理推荐


3156医药网APP